BIOLOGIJA
Antidijabetici. Pomama za novim lijekovima koji značajno pomažu smanjiti tjelesnu težinu
 Tamara Čačev / 13. siječnja 2023. / Perspektive / čita se 12 minuta
Tamara Čačev / 13. siječnja 2023. / Perspektive / čita se 12 minuta

 Tamara Čačev / 13. siječnja 2023. / Perspektive / čita se 12 minuta
Tamara Čačev / 13. siječnja 2023. / Perspektive / čita se 12 minuta

Nova klasa antidijabetika, razvijenih u prošlom desetljeću, ima snažan odjek u medijima otkako su kliničke studije pokazale kako imaju značajan učinak na smanjenje tjelesne mase, piše Tamara Čačev. Potražnja je tolika da je Novo Nordisk lani uložio 1,6 milijardi dolara u gradnju tri proizvodna pogona kako bi zadovoljio potrebe tržišta.
Izobilje hrane u svako doba dana i noći relativno je recentna blagodat ljudskog roda, barem u razvijenim dijelovima svijeta. Takva raskoš nije dostupna gotovo niti jednom drugom živom biću, no nažalost naš organizam nije programiran za funkcioniranje u takvim uvjetima. Naše donedavno “prirodno” stanje bilo je da nam hrana nije uvijek dostupna, pogotovo ne visoko procesirana kalorijski nabijena hrana. Stoga su naše metaboličke funkcije podešene da iskoristimo priliku i najedemo se kad nam se posreći (sjetite se švedskih stolova) i da to pospremimo u mast za “zlu ne trebalo” jer tko zna hoće li i sutra biti takve prilike. Još bi to možda i imalo smisla kada bismo naporno fizički radili, kopali na polju ili radili u rudniku, no svi znamo kakva je većina poslova današnjice, naravno u razvijenom svijetu. To je ukratko recept za nastanak inzulinske rezistencije (o kojoj sam pisala u jednom od prethodnih tekstova) i metaboličkog sindroma koji dovode do dijabetesa tipa dva, povišenog krvnog tlaka i masne jetre, a u konačnici i do bolesti kardiovaskularnog sustava koji su tihi ubojice modernog čovjeka.
Sve mi to danas znamo, no što poduzeti? Manje jesti i više se kretati. E, kad bi to bilo tako jednostavno, onda i ne bismo došli u ovakve probleme. Istina je da se svakako moramo potruditi i aktivirati snagu volje (u onoj mjeri u kojoj nam ju je priroda podarila) no moramo biti pošteni i priznati da nije sve u “htjeti”, pogotovo u osoba koje imaju stvarni osjećaj gladi uzrokovan objektivnim endogenim čimbenicima. Također nije ni sve u paroli: calories in-calories out koju jako vole fitness treneri. Jasno je da fizikalni zakoni vrijede i u procesu dobivanja i gubitka tjelesne mase i da ako unosimo manje kalorija nego trošimo moramo izgubiti na težini. No, biokemijski i metabolički procesi koji dovode do gomilanja zaliha u masnom tkivu ne odvijaju se mehanizmima koji su reverzibilna slika kada te kalorije treba potrošiti. Također, u osoba u kojima su ti mehanizmi pohrane i trošenja energije disfunkcionalni, fizikalna načela postaju manje presudna zbog objektivne biološke ‘pomaknutosti’ sustava da preferira drugačiju vrstu ravnoteže.

Jedan od najočitijih bioloških mehanizama koji bi morao kontrolirati našu tjelesnu masu jest osjećaj sitosti i gladi. Kada su ova dva mehanizma dobro ugođena, osoba jede točno toliko koliko joj je potrebno da se postigne osjećaj sitosti i zadovolji osjećaj gladi. No problem nastaje kada su ti mehanizmi pomaknuti, primjerice u smjeru gladi, iako je unešena hrana objektivno dovoljna za podmirenje energetskih potreba. Uzroci prejedanja su mnogostruki, dijelom ulaze i u domenu psihologije, no ako zanemarimo subjektivne razloge koji nas tjeraju da pojedemo više nego što bi bilo optimalno, još nam ostaju stvarni učinci hormona koji reguliraju taj naš osjećaj sitosti i gladi te ako su oni izvan balansa osoba osjeća vrlo stvarni i neizdrživi poriv za hranom.
U ovim procesima dominantnu ulogu imaju inkretini, hormoni koji se otpuštaju iz enteroendokrinih stanica crijeva u krvotok kao odgovor na unos hrane u svega nekoliko minuta nakon obroka. Njihova zadaća je da moduliraju sekretorni odgovor inzulina na nutrijente iz hrane. To su dakle molekule koje se luče u probavnom sustavu i reguliraju osjećaj gladi i sitosti kao i razinu odgovora na unos glukoze. Taj sekretorni odgovor naziva se još i inkretinskim efektom te čini više od 50% ukupnog inzulina koji se luči nakon uzimanja hrane. Radi se o opaženom fenomenu u kojem glukoza koja je u organizam unešena putem hrane ima snažniji učinak u otpuštanju inzulina u odnosu na učinak glukoze administrirane direktno u krvotok pri jednakoj razini glukoze u krvi. Kod zdravih osoba ovaj inkretinski učinak odgovoran je i za do 70% lučenja inzulina nakon obroka.
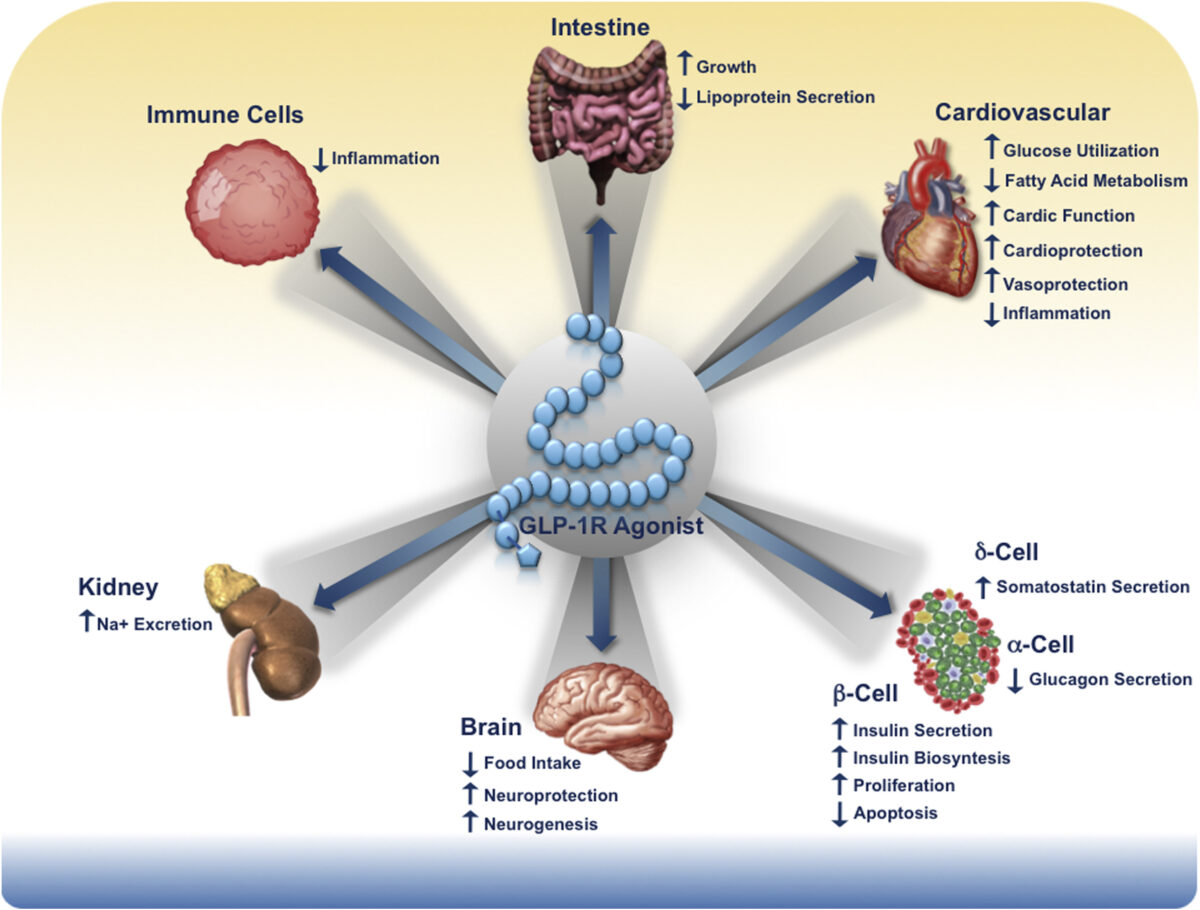
Dakle, moglo bi se reći kako su inkretini zapravo inzulinotropni hormoni budući da potiču izlučivanje inzulina nakon obroka. Cilj ovog lučenja inzulina jest da se glukoza dobivena iz hrane distribuira u stanice kako bi služila kao pogonsko gorivo za njihov rad. U osoba koje su zdrave porast glukoze nakon obroka prati i porast inzulina te se time razina glukoze u krvi smanjuje a zatim se zaustavlja i lučenje inzulina.
Iako ideja o inkretinskom učinku, tj. o lučenju hormona nakon unosa hrane nije nova, molekule koje sudjeluju u ovim procesima otkrivene su relativno nedavno zahvaljujući napretku molekularne biologije. Danas poznajemo dva glavna inkretina, nazvana opisno prema njihovoj funkciji te je stoga direktni prijevod na hrvatski pomalo nezgrapan a radi se o inzulinotropnom peptidu ovisnom o glukozi (GIP, od engl. glucose-dependent insulinotropic peptide) otkrivenom 1971.godine, te peptidu koji nalikuje glukagonu 1 ( GLP-1, od engl. glucagon-like peptide-1) otkrivenom 1985.godine. GIP se sintetizira u enteroendokrinim stanicama (tzv. K stanice) u početnom dijelu tankog crijeva dok se GLP-1 sintetizira u enteroendokrinim stanicama (tzv. L stanice) u tankom crijevu i početnom dijelu debelog crijeva.
Oni imaju niz zajedničkih djelovanja u gušterači no imaju različite uloge u drugim dijelovima organizma (slika dolje). Sve svoje funkcije obavljaju putem vezanja na svoje receptore koji se nalaze na stanicama gušterače ali i u drugim tkivima u organizmu. Oba se brzo deaktiviraju uz pomoć enzima dipeptidil peptidaze 4 (DPP4). Ovaj enzim nalazi se na površini limfocita te endotelnih stanica krvnih žila i aktivira se nakon otpuštanja GIP i GLP-1 u krvotok čime zaustavlja inkretinski odgovor.
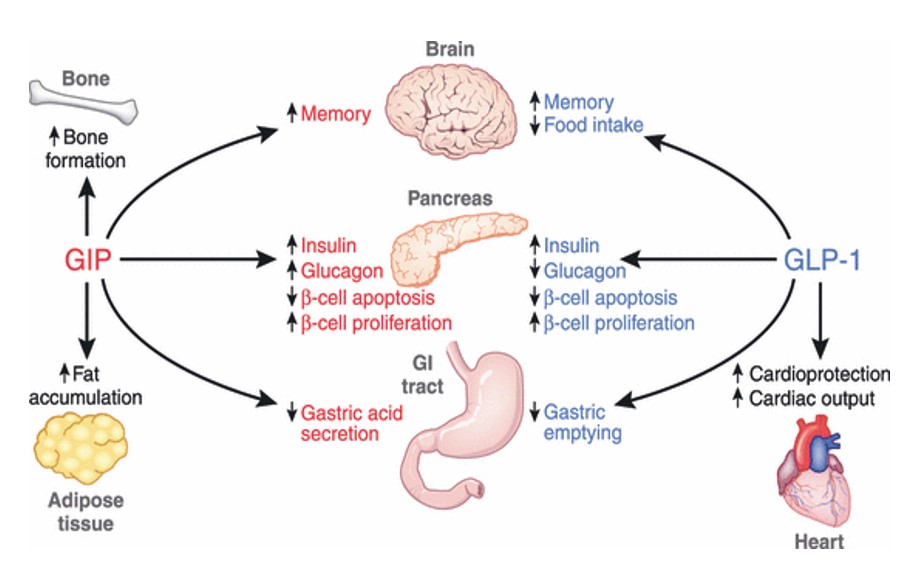
Uz inzulinotropno djelovanje GIP također sudjeluje i u metabolizmu masti u masnim stanicama te pojačava sintezu triglicerida iz masnih kiselina pod utjecajem inzulina, zatim stimulira aktivnost lipoprotein lipaze te na niz drugih načina utječe na sintezu masnih kiselina. GLP-1 osim inzulinotropnog učinka također inhibira pražnjenje želuca, smanjuje uzimanje hrane, inhibira sekreciju glukagona te snižava brzinu nastanka endogene glukoze, što sve pozitivno djeluje na snižavanje razina glukoze u krvi u oboljelih od dijabetesa tipa 2. Primarni fiziološki poticaj za izlučivanje GLP-1 su obroci bogati mastima i ugljikohidratima, no stimuliraju ga i obroci koji sadrže uz glukozu i druge šećere, umjetne zaslađivače, masne kiseline, aminokiseline te vlakna. Otuda dolaze i ideje kako primjerice gazirana pića zaslađena umjetnim sladilima također utječu na inzulinski odgovor te mogu izazvati poremećaje u njegovoj regulaciji.
I GLP-1 i GIP izazivaju inkretinski učinak no u njemu dominantnu ulogu (do 2/3 učinka) ipak ima GIP u zdravih osoba. Kod osoba s dijabetesom tipa 2 inkretinski učinak je poremećen što dovodi do neadekvatne kontrole postprandijalne razine glukoze u krvi. U tih osoba, GIP više ne modulira sekreciju inzulina ovisnu o glukozi čak i pri njenim vrlo visokim koncentracijama u plazmi te je stoga ta njegova nefunkcionalnost pogubna za funkciju beta-stanica gušterače, pogotovo nakon obroka. Točan uzrok zašto se to događa nije još razjašnjen. No, istovremeno GLP-1 i dalje ima inzulinotropni učinak i stoga se došlo do ideje da bi se možda agensima koji imitiraju njegov učinak na receptor moglo poboljšati inzulinsku sekreciju. To je dovelo do prve generacije lijekova koji su se temeljili na inkretinskom učinku a registrirani su tijekom prve dekade ovog stoljeća kao terapija za snižavanje razina glukoze u oboljelih od dijabetesa tipa 2. Radilo se o eksenatidu, dugodjelujućem agonistu GLP-1 receptora te sitagliptinu koji je inhibitor enzima DPP4. Sredinom druge dekade ovog stoljeća odobren je još jedan lijek temeljen na aktivnom agensu liraglutidu koji je postizao gubitak tjelesne mase od 8% u odnosu na placebo.
Učinak je spektakularan. Dok se korištenjem prijašnjih lijekova postizao gubitak tjelesne mase od 5-10%, nova klasa agenasa postiže učinke od 15-20% u godini dana ovisno o dozi.
Na principima regulacije inkretinskog učinka temelji se i nova klasa antidijabetika koja je razvijena u proteklom desetljeću i koja u poslijednje vrijeme ima značajan odjek u medijskom prostoru. Taj nagli porast interesa krenuo je početkom 2021. godine kada su izašli rezultati treće faze kliničke studije nove klase antidijabetika, modificirane verzije liraglutida nazvane semaglutid koja je u tijelu ostajala dulje i tako imala bolji i dugotrajniji učinak. Iako je prvotno razvijen kao lijek u terapiji dijabetesa tipa-2, kroz kliničke studije utvrđeno je kako ima i značajan učinak na smanjenje tjelesne mase. To je pokrenulo istraživanja na nekoliko frontova u cilju optimizacije peptida sa što boljom funkcijom agonista inkretinskog učinka. Zatim su nakon registracije za liječenje dijabetesa tipa-2 pokrenute kliničke studije njihovog djelovanja na pretilost te su neki od njih registrirani i za tu primjenu tijekom 2022. godine (Novo Nordisk) a tijekom ove godine očekuje se odobrenje za još neke (Elly Lilly).
Učinak ove nove generacije inkretinskih agonista je spektakularan. Dok se korištenjem prijašnjih lijekova postizao gubitak tjelesne mase od 5-10%, nova klasa agenasa postiže učinke od 15-20% gubitka tjelesne mase u godini dana ovisno o dozi. Rijetko se u razvoju lijekova dogodi da neki daje tako vidljive i relativno brze učinke, stoga ne čudi kako je već i prije njihove registracije za tretiranje pretilosti zavladala pomama i među zdravim osobama s viškom kilograma, najprije u SAD a zatim i u ostatku svijeta.
Prva ciljna molekula na koju je razvijen novi tip terapije bio je GLP-1, koji ima bitnu ulogu u kontroli tjelesne mase kroz utjecaj na mozak i probavni sustav. Više razine GLP-1 izazivaju manji osjećaj gladi te dulji osjećaj sitosti što naravno pomaže u dosezanju ultimativnog cilja a to je gubitak tjelesne mase. Prvi odobreni preparat za liječenje pretilosti sadržavao je semaglutid koji je prvotno registriran kao antidijabetik koji kontrolira i pojačava učinak GLP-1 kroz djelovanje na njegov receptor (dakle radi se o agonistu GLP-1 receptora). Lijek je 2021. godine odobren i u svrhu terapije pretilosti te se administrira u obliku injekcije jednom tjedno. Kada se koristi kao lijek za dijabetes Novo Nordiskov preparat se prodaje u nižim koncentracijama pod komercijalnim nazivom Ozempic dok se primjenu u smanjenju tjelesne mase koriste više doze pod komercijalnim nazivom Wegovy.
Sljedeća u nizu novih molekula bio je tirzepatid, peptid koji uz djelovanje na GLP-1 također utječe i na GIP kroz aktiviranje oba receptora. GLP-1 i GIP imaju sinergističko djelovanje tako da tirzepatid djelovanjem na obje ciljne molekule ima još značajniji učinak na gubitak tjelesne mase (u dozi od 15 mg postizan je u kliničkoj studiji gubitak tjelesne mase od skoro 21% u 72 tjedna ispitivanja). Tirzepatid je peptid čiju okosnicu čini sekvenca aminokiselina preuzeta iz GIP ali je na nju dodan i dio koji se može vezati i na GLP-1 receptor. Komercijalni pripravak koji je prvi stigao na tržište je Elly Lillyev Mounjaro. Tirzepatid u ovom preparatu ima slabiji afinitet za GLP-1 receptor u odnosu na GLP no ima podjednak afinitet za GIP receptor kao i nativni ligand hormon GIP. U osoba s dijabetesom tipa 2 ovaj preparat poboljšava regulaciju glikemijskog statusa kroz nekoliko djelovanja. Potiče sekreciju inzulina te suprimira sekreciju glukagona. Također poboljšava osjetljivost stanica na inzulin. Konačno, kroz djelovanje na mozak i probavni sustav smanjuje potrebu za unosom hrane te usporava pražnjenje želuca. I ovaj se preparat administrira u obliku injekcije jednom tjedno i trenutno je odobren kao antidijabetik za dijabetes tipa 2 no u ovoj godini očekuje se i odobrenje za njegovu primjenu u liječenju pretilosti.
Kao nuspojave uzimanja nove klase lijekova navedene su probavne smetnje u vidu mučnina, proljeva ili zatvora. Puno ozbiljnije ali zasad nasreću rjeđe nuspojave su pankreatitis, akutno zatajenje bubrega te bolesti žučnog mjehura. Tijekom ispitivanja na laboratorijskim štakorima, tirzepatid je izazivao tumore štitnjače što zasad nije utvrđeno u kliničkoj studiji provedenoj na ljudima. Ipak, zbog toga je kontraindiciran za primjenu u osoba s medularnim karcinomom štitnjače te sindromom MEN-2 (sindrom multiple endokrine neoplazije tipa 2) u osobnoj ili obiteljskoj anamnezi.
Jedna od negativnih strana ovih novih terapija jest njihova cijena koja iznosi oko 1500 dolara mjesečno i nije pokrivena zdravstvenim osiguranjem u većini država ako se radi o lijeku koji se koristi isključivo u svrhu smanjenja tjelesne mase. O koliko se velikom novcu radi govori i činjenica da je Novo Nordisk 2022. godine uložio preko 1,6 milijardi dolara u izgradnju tri proizvodna pogona kako bi se zadovoljile enormno rastuće potrebe za ovim preparatima. No, ulaskom ovih terapija u širu primjenu očekuje se i njihovo pojeftinjenje i refundacija od zdravstvenih osiguranja budući da se smanjenjem tjelesne mase smanjuje rizik za čitav niz drugih bolesti što bi u konačnici trebalo rezultirati manjim troškovima. U najavi su i drugi agonisti GIP i GLP-1 te tzv trostruki agonisti koji bi uz ova dva inkretina imitirali i djelovanje glukagona.
Ipak, nakon smanjenja tjelesne mase i prekida terapije, izazov je održati takvo stanje bez terapije i vraćanja izgubljenjih kilograma. Stoga se i u protokolima primjene ovih lijekova navodi kao primarni uvjet pravilna prehrana i tjelovježba te se ova terapija zapravo smatra samo dodatkom kako bi se poboljšala kontrola glukoze u krvi. Također tek treba vidjeti hoće li sve osobe jednako reagirati na terapiju jer se već sada primjećuje kako su ovi lijekovi manje učinkoviti na smanjenje tjelesne mase kod osoba koje već boluju od dijabetesa tipa 2. Stoga ne treba misliti kako su oni magično rješenje svih naših problema s tjelesnom težinom jer je upitno koliko je to financijski a i zdravstveno dugoročno održivo budući da je kontrola tjelesne mase za mnoge od nas cjeloživotna borba.
1) Nauck MA, Meier JJ (2018). Incretin hormones: Their role in health and disease. Diabetes Obes Metab. Suppl 1:5-21.
2) Rehfeld JF (2018) The Origin and Understanding of the Incretin Concept Front. Endocrinol.Sec. Cellular Endocrinology. 9:387.
3) Prillapman M (2023). The showstopper obesity drugs that have stunned the researchers. Nature 613:16-18.