Nobelova nagrada za medicinu i fiziologiju 2021
Lahor na licu, nježnost dodira. Što su to važno otkrili ovogodišnji nobelovci.
 Tamara Čačev / 8. listopada 2021. / Perspektive / čita se 14 minuta
Tamara Čačev / 8. listopada 2021. / Perspektive / čita se 14 minuta

 Tamara Čačev / 8. listopada 2021. / Perspektive / čita se 14 minuta
Tamara Čačev / 8. listopada 2021. / Perspektive / čita se 14 minuta

Tek kad se uđe u pojedinosti otkrića za koje su ovogodišnji nobelovci za medicinu i fiziologiju dobili nagradu spozna se koliko su čovjek i život uopće složeni. Osjeti nisu samo oni na koje prvo pomislimo, njuh, vid, sluh, okus. Kako osjetimo nježnost kože i toplinu od uzbuđenja, zube protrnule od hladne vode objašnjava Tamara Čačev
Nobelova nagrada za fiziologiju ili medicinu ove je godine, unatoč nekim drugim predviđanjima koja su tipovala na neke od znanstvenika čija su nam otkrića omogućila brzi razvoj cjepiva protiv SARS-CoV-2, pomalo izvan reflektora medija otišla u ruke dvojici znanstvenika koji su opisali kako na molekularnoj razini funkcionira osjet dodira i topline.
Kada je Afred Nobel u svojoj oporuci definirao kriterije za otkrića dostojna nagrade koja nosi njegovo ime, a to je bilo još u pretprošlom stoljeću 1895.godine, nije mogao niti slutiti kuda će nas znanost novog doba odvesti. No njegovi kriteriji su i danas primjenjivi jer su univerzalni, naime nagrada se ima dodijeliti „onima čije otkriće tijekom prethodne godine donese najveću dobrobit za čovječanstvo“. Iskustvo nekih početnih nagrada je pokazalo kako se s vremenskim kriterijem ipak mora biti malo fleksibilniji budući da se za rijetko koje otkriće u prvim godinama jasno vidi cjelokupni doprinos za čovječanstvo. Tako je bilo i nekih (rijetkih) nagrada koje je vrijeme opovrgnulo. No, kriterij dobrobiti za čovječanstvo, u smislu otkrića koje je otvorilo nova vrata ili dalo novi pogled na neki znanstveni problem, dakle promijenilo paradigmu, prilično je jasno postavljen. U tome smislu tijelo koje odabire dobitnike okrenuto je više prema fundamentalnim pomacima u znanosti kojima se širi obzor cjelokupnog znanja koje ljudski rod posjeduje. Tek protok vremena pokazuje hoće li ova otkrića imati i neku konkretnu praktičnu komponentu. Stoga se obično ne žuri s recentnim otkrićima, no također se vodi računa i o dobi potencijalnih laureata budući da se nagrada dodjeljuje živućim znanstvenicima.
Stoga je interesantno kako ovogodišnji laureati za nagradu u području medicine ili fiziologije nisu u poodmakloj životnoj dobi niti je njihova nagrada, barem u slučaju jednog od njih, bila dugo iščekivana. Radi se o profesorima Davidu Juliusu sa Sveučilišta u Kaliforniji i Ardemu Patapoutianu s Medicinskog instituta Howard Hughes koji su nagradu dobili za otkriće receptora za toplinu (na početku 2000-tih) odnosno dodir (2010.-2015.g).
Iako smo mi ljudi kao vrsta svoj opstanak na Zemlji zahvaljujući razvoju našeg mozga učinili poprilično neovisnim o neposrednim životnim ugrozama koje vrebaju druge životinje, još smo itekako ovisni o informacijama koje dobivamo iz svoje okoline ali i vlastitog organizma. Ove informacije do našeg mozga dolaze putem živčanog sustava sa receptora koji se najčešće nalaze na površini našeg tijela no ovisno o funkciji imamo ih i u našoj unutrašnjosti. Vid, sluh, njuh, okus, kojih se nekako najprije sjetimo kada je riječ o osjetima, u modernom suportivnom svijetu više ne predstavljaju čimbenike koji, ako se oštete, postaju životno ugrožavajući kako je to slučaj u drugim životinjskim vrstama. No postoje i druge vrste osjeta kojih možda nismo ni toliko svjesni a zapravo su esencijalni za naše preživljavanje poput osjeta dodira, boli ili osjeta hladnoće i topline ili boli.
Osjet dodira koji je u osnovi detekcija mehaničke sile daje nam sposobnost prepoznavanja tekstura, veličina i oblika predmeta kao i osjet vibracija. Omogućava da osjetimo mekoću brašna ili povjetarac na licu. Sve su to osjeti koji se na našoj koži rasčlanjuju i registriraju kao niz pojedinačnih stimulusa poput udubljenja/rastezanja na površini kože, savijanja dlake ili njene vibracije i svaki od tih stimulusa aktivira drugi tip senzornih neurona koji se tek centralno integriraju u neku od spomenutih senzacija.
U tjelesne osjete spada i osjet boli koje izazivaju stimulusi koji aktiviraju posebni tip živčanih vlakana (nociceptori) kao odgovor na jaku mehaničku silu ili bolnu toplinu. Ovi nam receptori daju informacije o opasnostima u našoj okolini poput primjerice vruće vode ili hladnoće za zube pri dodiru s ledom a sve radi sprečavanja oštećenja tkiva i aktivacije refleksa uzmaka. Pijenje vode tako postaje kompleksna radnja u kojoj naši osjetilni neuroni prenose informaciju o težini, veličini, teksturi i temeperaturi tekućine i čaše iz koje pijemo kako bi mogli primijeniti adekvatni stisak ruke i koordinirano ispiti gutljaj. To su sve radnje, poput hodanja ili održavanja ravnoteže kojih nismo niti svjesni a istovremeno se ogromna količina informacija generira i procesira u našem mozgu kako bi se adekvatno odradio idući korak. Koliko su ovi sustavi bitni postajemo svjesni tek kada nam u bolesti neka od ovih funkcija više ne ide glatko kako smo navikli.
O osjetu njuha i kako dolazi do pretvorbe mirsnog signala u signal koji naš mozak pretvara u smislenu informaciju pisala sam nedavno. No u svojoj osnovi svi osjeti prate sličnu shemu prijenosa signala. S jedne strane imamo podražaj koji može biti svjetlosni, kemijski, mehanički ili toplinski i taj se osjet zatim pretvara u živčani impuls kojeg naš mozak pretvara u smislenu informaciju po kojoj zatim djeluje bilo svojim svjesnim bilo nesvjesnim dijelom. U animalnoj fiziologiji se ova shema kristalizirala već relativno rano u začecima moderne fiziologije, no sami receptori pojedinog osjeta i molekularni mehanizmi kojima se signal iz okoliša pretvara u receptorskim stanicama u živčani impuls razotkriveni su u proteklih stotinjak godina te su kroz vrijeme ovjenčani s nekoliko Nobelovih nagrada. Stoga je sada možda jasniji i kontekst u kojem je išlo promišljanje odbora koji odabire dobitnike ove nagrade.

Kako sam već spomenula, idejni koncept o tome kako osjećamo podražaje različitih osjeta postojao je već u 17. stoljeću kada je Descartes zamišljao niti koje povezuju različite dijelove kože s mozgom, a priroda tih niti, danas znamo da je riječ o neuronima, rasvijetljena je tek kasnije. U tome je značajnu ulogu imao niz znanstvenika od kojih su neki za svoja otkrića dobili i Nobelove nagrade. Prvi u tome nizu bili su Camillo Golgi i Santiago Ramón y Cajal 1906.g za zasluge u opisivanju osjetilnog dijela živčanog sustava koji je uključivao i anatomski opis somatosenzoričkog sustava. Zatim su 1932. g. Charles Sherrington i Edgar Adrian dobili Nobelovu nagradu za opisivanje funkcije neurona uključujući i somatosenzoričke neurone. Konačno su 1944. godine ovu nagradu dobili Erlanger i Gasser jer su po prvi put pokazali kako postoje različiti tipovi senzoričkih živčanih vlakana koje mogu registrirati točno određene tipove podražaja i promjena u okolini. Osjet topline odnosno dodira s nečim vrućim, osjet različitih tekstura koje raspoznajemo pod prstima, osjet boli i pritiska bitni su za naše preživljenje.
Ovim otkrićima utvrđeni su temeljni postulati širenja akcijskih potencijala duž senzornih živaca u mišićima i na koži. Otkriće različitih tipova živčanih vlakana s različitom brzinom provođenja signala kao i različitim pragom aktivacije i refraktornim periodima omogućilo je da se specifični tip vlakna poveže sa pojedinim tipom osjeta poput dodira ili osjeta topline. Ali priroda i molekularna osnova receptora koji osjećaju toplinu i dodir te kako se ti signali pretvaraju u akcijske potencijale u živčanim vlaknima bila je i dalje misterij.
No, vratimo se na meritum otkrića ove dvojice znanstvenika, kako su oni, svaki u svojem području razotkrili kako se toplinski i mehanički podražaj pretvaraju u živčani impuls.
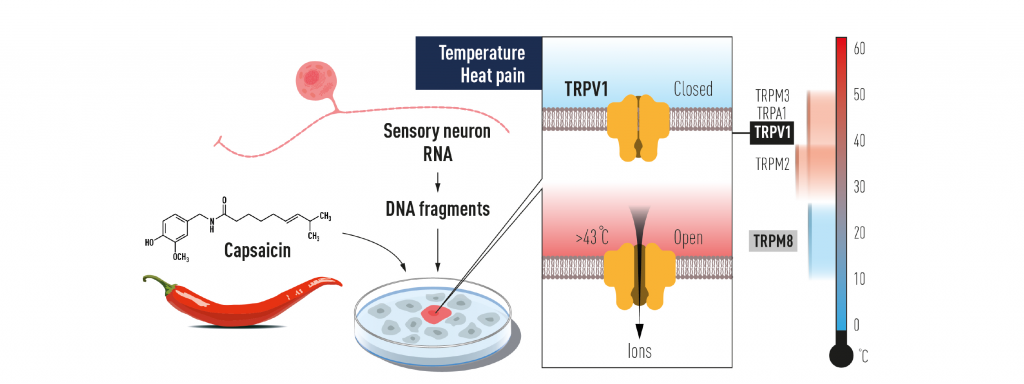
Prof. Julius je potkraj 90-tih i početkom 2000.-tih u nekoliko temeljnih radova prikazao kako zapravo funkcionira osjet za toplinu i hladnoću. U svojim eksperimentima koristio je kapsaicin, spoj koji nam je poznat kao ljutina koju osjećamo kad okusimo chilli papričice. Na prvu se čini kako ljutina nema možda previše veze s osjetom toplo/hladno, no ako se prisjetimo osjećaja žarenja na koži kakvo izaziva ovaj spoj počinje se nazirati razlog kako je on poslužio za otkrivanje senzora upravo za toplinu. Svima je poznato kako izrazito ljuta hrana začinjena chillijem izaziva znojenje –fenomen koji je 50-tih godina prošlog stoljeća opisan kao gustatorno znojenje. Tijekom vremena utvrđeno je kako kapsaicin djeluje direktno na osjetilne živce i izaziva strujni impuls koji se manifestira kao osjet topline koji ide sve do boli. Početna ideja da neki kemijski spoj može izazvati osjećaj boli bila je premisa daljnjeg istraživanja upravo senzornih neurona koji reagiraju na bol, toplinu i dodir. Kako bi otkrili koja je to točno molekula, receptor na površini neurona, odgovorna za primanje ovog signala Dr. Julius i njegovi suradnici analizirali su ekspresiju svih aktivnih gena u tim neuronima. Izolirali su mRNA iz stanica (daju je samo oni geni koji su aktivni što je manji postotak svih gena u genomu) i preveli je u cDNA oblik koji je lakši za daljnju manipulaciju. Zatim su napravili svojevrsnu ‘knjižnicu’ fragmenata DNA koji su u sebi nosili gene te su ih pojedinačno analizirali u kulturi stanica koje u normalnim uvjetima ne reagiraju na kapsaicin. Nakon dugotrajnog i opsežnog screeninga svakog od fragmenata DNA iz knjižnice uspjeli su identificirati gen koji stanice čini osjetljivima na kapsaicin. Radilo se o do tada neopisanom receptoru koji služi kao ionski kanal a koji je kasnije nazvan TRPV1 budući da je analizama homologije utvrđeno da pripada superfamiliji TRP ( engl. transient receptor potential) kationskih kanala.
Zatim je ovaj protein u uvjetima in vitro testiran na to da li stanicama u kojima je eksprimiran daje mogućnost odgovora na toplinu te se ubrzo shvatilo kako se uistinu zapravo radi o receptoru koji može osjetiti toplinu i aktivira se pri temperaturama koje nam izazivaju osjet boli (iznad 40°C, što je blizu psihološke granice boli). Nakon niza eksperimenata pokazalo se da ovaj receptor djeluje kao molekularni integrator signala bolne topline ali i kemijskih stimulansa poput spoja iz chilli papričica.
Kasnije je otkriven i niz drugih receptora koji su aktivni u drugačijim temperaturnim rasponima (slika 1). Primjerice TRPA1 reagira na čitav niz vanjskih stimulusa poput ulja goruščice, hrena, cimeta, češnjaka i đumbira čiji osjet ide gotovo do boli. No ovaj receptor također reagira i na toplo i na hladno. Drugi otkriveni receptor TRPM2 je odgovoran za osjet u rasponu od 33 do 38 °C.
Osjet hladnoće kod čovjeka počinje pri 28°C i vrlo precizno razaznajemo razlike od svega pola stupnja. Interesantno je kako su neovisno jedan o drugom i Julius i Patapoutian koristili istu kemijsku tvar, mentol kao kemijski stimulans koji u ljudi izaziva i osjet hladnoga kako bi 2002.g otkrili isti receptor TRPM8 kojeg aktivira hladnoća.
Između 2010. i 2015. g prof. Patapoutian u nekoliko je radova prikazao je svoja otkrića u području receptorskih stanica osjetljivih na pritisak. Otkrio je novi tip senzora koji odgovara na mehanički podražaj na površini našeg tijela ali i iz njegove unutrašnjosti, što je također bitno kako bi se dobila kompletna informacija o funkcionalnosti naših unutarnjih sustava. No, kako uopće pristupiti rješavanju ovog problema, kako ispitati da je neka stanica osjetljiva na mehanički pritisak? Trebalo je najprije pronaći staničnu liniju adekvatnu za rad na ovakvom problemu. U tome su Patapoutian i suradnici uspjeli kada su pronašli stanice Neuro2A koje su odavale mjerljivi električni impuls na pritisak pipetom. Pretpostavili su kako je u tim stanicama moralo doći do aktivacije receptora koji osjeća mehanički pritisak te da se najvjerojatnije mora raditi o proteinu tipa ionskog kanala jer su uglavnom takvi proteini angažirani u generiranju živčanog impulsa. Stoga su analizirali genom tih stanica i utvrdili da postoji 72 potencijalna gena koji kodiraju za ionske kanale. Zatim su dugotrajnim i zahtjevnim eksperimentalnim pristupom metodom RNA interferencije inaktivirali jedan po jedan od ovih gena u analiziranim stanicama kako bi otkrili koji je odgovoran za osjet mehaničkog pritiska. Naravno, stanica koja bi se pokazala neosjetljiva bila bi upravo ona u kojoj se nalazi gen koji je za taj proces bitan ali je inaktiviran. Tako je otkriven novi tip mehanoosjetljivih ionskih kanala Piezo 1. Zatim je u pokusima ektopičke ekspresije u HEK-293 stanicama koje nisu mehanoosjetljive pokazano kako one to postaju kada im se ubaci gen PIEZO1. Pretraživanjem genoma pronađen još jedan vrlo sličan gen nazvan Piezo 2. Za oba ova receptora se kasnijim eksperimentima nedvojbeno dokazalo da dolazi do njihove aktivacije kada se na membranu stanice izvede mehanički pritisak (slika 2).
Piezo proteini predstavljali su sasvim novi tip mehanosenzitivnih kanala kod kralježnjaka a radi se o najvećim ikad opisanim transmembranskim proteinima koji kroz membranu prolaze čak 38 puta i imaju više od 2500 aminokiselina u podjedincama. Mehanizam kako točno mehanička sila otvara centralnu poru ovog kanala još nije razjašnjen.
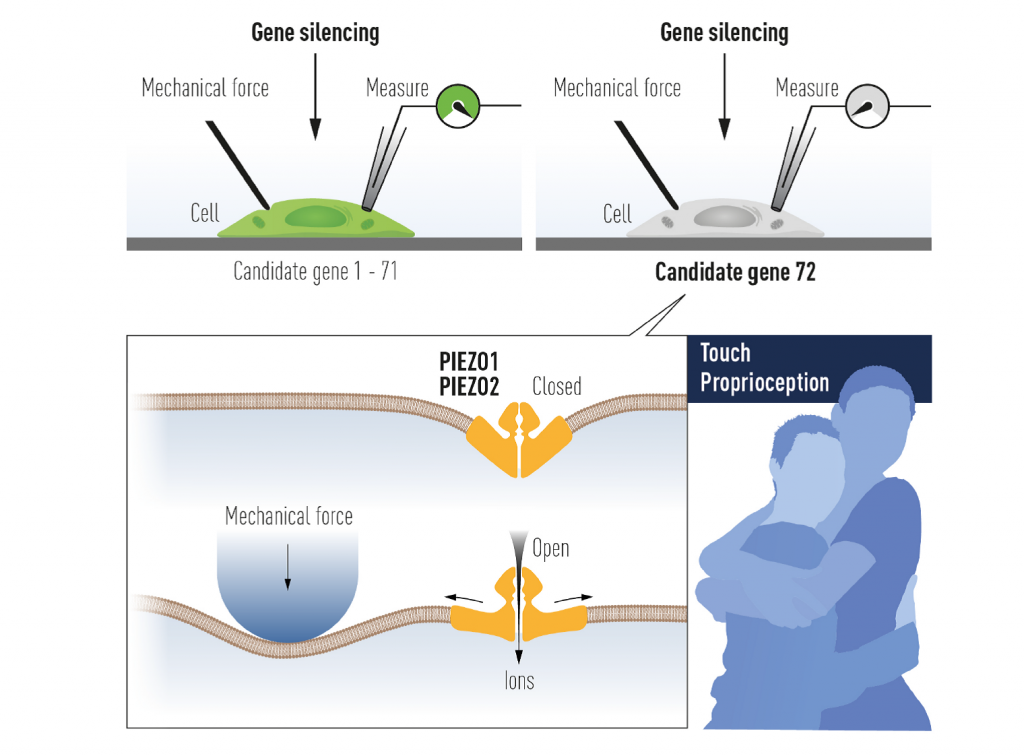
Daljnjim istraživanjima se pokazalo kako je zapravo Piezo 2 kritičan za osjet dodira te za percepciju pokreta i položaja dijelova tijela u prostoru – propriocepciju. Za razliku od klasičnih osjetilnih receptora koji su nam poznati na površini tijela, proprioceptori su smješteni u našoj nutrini, u zglobovima, mišićima, tetivama i ligamentima. Također se pokazalo kako ova dva receptora sudjeluju u nekoliko bitnih fizioloških procesa poput regulacije tlaka, disanja te kontrole mokraćnog mjehura što su sve procesi u kojima je bitan osjet pritiska na stanice koje oblažu krvne žile i unutarnje organe. U plućima Piezo 2 djeluje kao receptor koji prepoznaje rastezanje stijenke bronha i bronhiola do čega dolazi jakim udahom i tada dolazi do aktivacije protektivnog refleksa koji štiti pluća od pretjeranog napuhavanja. Barorefleks u arterijama kontinuirano prati i održava krvni tlak a informacije dobiva od Piezo1 i 2. Piezo 2 kanal nam također omogućava da osjetimo dodir i imamo svjesnost o samome sebi u prostoru a esencijalni su i u procesu disanja, mokrenja, regulacije krvnog tlaka kao i remodeliranja našeg kostura, primjerice tijekom letova u svemir.
U humanoj medicini opisane su i neke rijetke genetske bolesti povezane s disfunkcijom TRP i Piezo kanala. Primjerice mutacije u TRPA1 izazivaju sindrom epizodne boli koji se manifestira s boli u gornjem dijelu tijela izazvanom hladnoćom. Neke varijante ovog gena povezane su i s neuropatskom boli i paradoksalnim osjetom topline. Mutacije u genu PIEZO2 u podlozi su nekoliko poremećaja koji se manifestiraju promjenama u osjetu dodita vibracija i propriocepcije.
Ujedinjeno ova otkrića omogućila su nam da shvatimo kako se toplina, hladnoća i mehanička sila pretvaraju u živčani impuls. No oni su također bitni za shvaćanje nekih patoloških stanja koja osjećamo poput upalne i kronične boli. Kako su ova područja još daleko od potpuno istraženih moguće je da će se s vremenom otkriti i nove uloge ovih receptora u patofiziologiji.
Caterina MJ, Schumacher MA, Tominaga M, Rosen TA, Levine JD, Julius D. The capsaicin receptor: a heat-activated ion channel in the pain pathway. Nature 1997:389:816-824.
Tominaga M, Caterina MJ, Malmberg AB, Rosen TA, Gilbert H, Skinner K, Raumann BE, Basbaum AI, Julius D. The cloned capsaicin receptor integrates multiple pain-producing stimuli. Neuron 1998:21:531-543.
Caterina MJ, Leffler A, Malmberg AB, Martin WJ, Trafton J, Petersen-Zeitz KR, Koltzenburg M, Basbaum AI, Julius D. Impaired nociception and pain sensation in mice lacking the capsaicin receptor. Science 2000:288:306-313
McKemy DD, Neuhausser WM, Julius D. Identification of a cold receptor reveals a general role for TRP channels in thermosensation. Nature 2002:416:52-58
Peier AM, Moqrich A, Hergarden AC, Reeve AJ, Andersson DA, Story GM, Earley TJ, Dragoni I, McIntyre P, Bevan S, Patapoutian A. A TRP channel that senses cold stimuli and menthol. Cell 2002:108:705-715
Coste B, Mathur J, Schmidt M, Earley TJ, Ranade S, Petrus MJ, Dubin AE, Patapoutian A. Piezo1 and Piezo2 are essential components of distinct mechanically activated cation channels. Science 2010:330: 55-60
Ranade SS, Woo SH, Dubin AE, Moshourab RA, Wetzel C, Petrus M, Mathur J, Bégay V, Coste B, Mainquist J, Wilson AJ, Francisco AG, Reddy K, Qiu Z, Wood JN, Lewin GR, Patapoutian A. Piezo2 is the major transducer of mechanical forces for touch sensation in mice. Nature 2014:516:121-125
Woo S-H, Lukacs V, de Nooij JC, Zaytseva D, Criddle CR, Francisco A, Jessell TM, Wilkinson KA, Patapoutian A. Piezo2 is the principal mechonotransduction channel for proprioception. Nature Neuroscience 2015:18:1756-1762