BIOLOGIJA
Ostarjeti što kasnije. Molekula koja bi mogla produžiti razdoblje zdravog života
 Tamara Čačev / 10. studenoga 2023. / Perspektive / čita se 12 minuta
Tamara Čačev / 10. studenoga 2023. / Perspektive / čita se 12 minuta
 Tamara Čačev / 10. studenoga 2023. / Perspektive / čita se 12 minuta
Tamara Čačev / 10. studenoga 2023. / Perspektive / čita se 12 minuta

Produljenje životnog vijeka bez produljenja perioda u kojem ćemo biti zdravi i funkcionalni nema smisla, piše Tamara Čačev u članku o rapamicinu, molekuli koja pokazuje velik potencijal u usporavanju starenja ljudi. Problem je što preostaje još mnogo naučiti o njoj, a istraživanja dugovječnosti na ljudima su izrazito komplicirana.
Rapamicin se, uz metformin, danas smatra jednom od molekula s najvećim potencijalom u postizanju dugovječnosti, odnosno kako se to stručnije kaže u tzv. geroprotekciji. Iako konačna presuda o djelotvornosti ovih molekula nije donesena, dapače u posljednje vrijeme se i rezultati čuvene studije o utjecaju metformina na trajanje životnog vijeka dovode u pitanje, to ne sprečava tech elitu sa zapadne obale SAD-a da ih koristi. Propagatori rapamicina, koji su većinom i poslovno vezani uz njegovo istraživanje, što svakako treba imati u vidu, tvrde kako ova molekula uz utjecaj na dugovječnost niza organizama na različitim stupnjevima evolucijske ljestvice uključujući miševe, pse pa onda moguće i ljude, uz utjecaj na produljenje životnog vijeka, također povoljno utječe i na produljenje perioda u kojemu smo zdravi (tzv. healthspan).
Ideja o supstanci koja bi trebala djelovati na produljenje života, odnosno usporavanje procesa starenja, ovisno o tome kako se na ove procese gleda, nije nova stvar. Već se pokazalo da metformin uz svoje djelovanje na šećernu bolest tipa 2 djeluje i na debljinu, metabolički sindrom te na sindrom policističnih jajnika. Acetilsalicilna kiselina (jedan od najpoznatijih komercijalnih preparata je Aspirin) smanjuje upalu a također djeluje i na smanjenje rizika od kardiovaskularnih bolesti i tromboze pa čak djeluje preventivno i na neke tipove tumora probavnog sustava. Takva polifunkcionalna djelovanja na više fronti svakako imaju potencijal produžiti nekome život te, da se ne radi o konvencionalnim supstancama koje već imaju svoju primjenu, mogli bismo ih nazvati geroprotektorima.
Što je od svega toga istina i je li to samo hype koji će proći? Kao što sam pisala u svom prethodnom tekstu o starenju, istraživanja dugovječnosti su izrazito kompleksna, teško je ekstrapolirati rezultate dobivene na miševima na potencijalni učinak supstanci na ljude. Sve i kad bi se mogao provesti izuzetno kontrolirani pokus dugogodišnjeg uzimanja neke od ovih tvari kao suplemenata, postavlja se pitanje što bi bila kontrola za takav pokus? Dugotrajnost takvog istraživanja, kao i potrebu sudjelovanja velikog broja ispitanika, bolje da i ne spominjemo. Znamo da se „na kraju bitke broje preživjeli“, i ova gruba prispodoba i u prenesenom i doslovnom smislu ipak najbolje ocrtava kompleksnost ovakvih istraživanja. Naravno, radi se i o ogromnim sredstvima koje bi trebalo uložiti u ova istraživanja, a dugovječnost nije primarni fokus većine državnih agencija koje financiraju znanstvena istraživanja. Stoga je zainteresiranost prije spomenutih milijunaša za ove teme od velikog značaja za razvoj ovog područja, no time se ujedno otvaraju i vrata za neortodoksne pristupe – kako istraživanjima tako i interpretaciji njihovih rezultata.
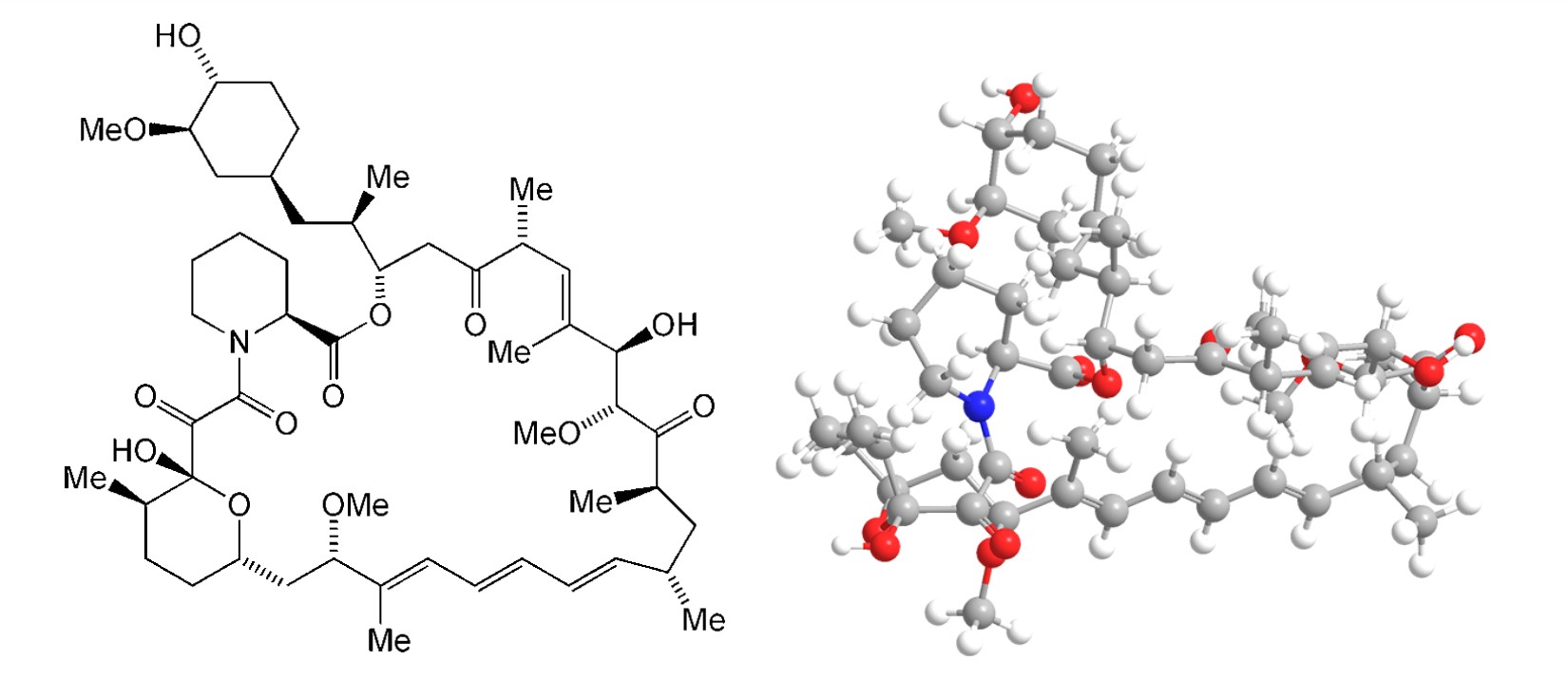
No, vratimo se rapamicinu, radi se o molekuli koja je otkrivena prije tridesetak godina i od onda se intenzivno istražuje njen učinak na različite aspekte staničnih funkcija. U posljednje vrijeme je medijski najeksponiraniji njen potencijal u mogućem usporavanju procesa starenja. Rapamicin djeluje kao inhibitor koji se veže na proteinske komplekse mTOR1 (i mTOR2) koji u stanici imaju ulogu svojevrsnih senzora razine nutrijenata, te regulira naš metabolički status, odnosno usmjerava stanice u fazu „izgradnje“ (anabolizam) ili „razgradnje“ (katabolizam) u ovisnosti o dostupnosti nutrijenata.
Interesantno je da je prvo otkriven rapamicin a tek potom njegova meta. Zanimljiva je i priča o njegovom otkriću. Otkriven je, naime, u uzorcima tla uzetim 70-tih godina s Uskršnjeg otoka (Rapa Nui) kojemu duguje i svoje ime. U tome se tlu nalazila bakterija Streptomyces hygroscopicus čiji je rapamicin produkt. Rapamicin spada u skupinu makrolida, spojeva koji imaju široko antibakterijsko djelovanje te je ovo svojstvo i bilo najprije opisano. Kasnije su otkrivena i njegova druga svojstva poput imunosupresije te je njegova prva klinički odobrena primjena (1999.) bila upravo u transplantacijskim protokolima u svrhu smanjenja mogućnosti odbacivanja transplantiranog organa. Ovakva primjena i doze koje su korištene bile su povezane s nizom ozbiljnih nuspojava u transplantiranih osoba te je stoga i rapamicin stekao donekle negativnu reputaciju. Od ove prvotne primjene prošlo je cijelo desetljeće prije nego li se ova supstanca počela istraživati i u drugim kontekstima, primjerice kao antitumorskog agensa ili molekule koja utječe na vitalnost i prolongiranje procesa starenja.
Od tada do danas provedena su mnoga istraživanja na nižim modelnim organizmima, kako djelovanja samog rapamicina, tako i posljedica genetičkog „onesposobljavanja“ njegove mete, mTOR-a te je pokazano kako duž cijelog evolucijskog spektra, s jedne strane rapamicin, a s druge strane i drugi načini ukidanja funkcije mTOR-a, mogu imati utjecaj na produžetak životnog vijeka u istraživanim životinjskim modelima. Činjenica da su biološki procesi starenja na razini stanice prilično konzervirani, a u biologiji to znači da su očuvani u nizu organizama na različitim stupnjevima evolucijskog razvoja, daje nadu da se otkrića provedena na miševima i C. elegans mogu barem donekle transponirati i na više sisavce pa tako onda potencijalno i ljude. Takav učinak pokazan je još jedino za kalorijsku restrikciju koja zapravo i gađa iste puteve koji povezuju metabolizam stanice s procesima koji su uključeni u njeno starenje.
Postavlja se pitanje zašto mi uopće i živimo toliko dugo jer smo jedna od rijetkih vrsta koja u reproduktivnoj i nerepoduktivnoj fazi provede gotovo podjednaki broj godina. U evolucijskom smislu svako održavanje organizma nakon reproduktivne faze nema previše smisla jer je on svoju ulogu izvršio te daljnje održavanje some (tijela) zapravo predstavlja samo enormni gubitak energije.
S druge pak strane postoje organizmi koji svoj životni ciklus završe u par tjedana ili mjeseci dok drugi žive i znatno dulje od nas, poput primjerice nekih kornjača. Prema današnjim spoznajama o molekularno-genetičkim mehanizmima koji sudjeluju u procesu starenja možemo identificirati njegovih 12 ključnih obilježja: nestabilnost genoma, skraćivanje telomera, epigenetske promjene u stanici, poremećaje ravnoteže razgradnje i sinteze proteina, onemogućavanje procesa „čišćenja“ staničnog smeća, poremećaj senzora za nutrijente, poremećaj rada staničnih energana- mitohondrija, prelazak stanica u stanje senescencije umjesto njihovog uklanjanja, iscrpljenost bazena matičnih stanica iz kojih se obnavljaju naša tkiva, poremećaji u komunikaciji između stanica te kronična upala i poremećaji mikrobioma.
Preko kojih signalnih puteva i na koje od ovih ključnih obilježja procesa starenja bi rapamicin mogao djelovati na dugovječnost?
Gledano načelno, mTOR, kojeg rapamicin inhibira, sudjeluje u čitavom nizu signalnih puteva i kada bi mu mogli dati jednu jedinu oznaku ona bi bila: „bitan regulator sinteze proteina“. To zapravo znači da, ukoliko ga inhibiramo, zapravo djelujemo na sve procese u stanici jer je za sve njih bitna sinteza proteina. Uz ovo općenito, globalno i nespecifično djelovanje mTORa, najizglednije se radi o njegovom utjecaju na autofagiju ili na kroničnu upalu. Na slici iznad je dan prikaz samo dijela kompleksne molekularne mreže na koju rapamicin djeluje. Ukratko možemo reći da se on veže na molekulu FKBP12 koju zapravo iskorištava kako bi se putem nje vezao na kompleks mTORC1 te ga blokirao i posljedično utjecao na procese autofagije i sinteze proteina te stanični metabolizam.
On zapravo priječi da se druge molekule vežu na aktivno mjesto mTOR1 ali ipak parcijalno, dakle neke funkcije mTOR1 ipak ostaju jer se neke molekule ipak i dalje mogu vezati. Nakon duljeg vremena rapamicin blokira i kompleks mTORC2, iako se prvotno mislilo da blokira samo mTORC1. Inhibicija mTORC2 smatra se odgovornom za većinu toksičnih nuspojava rapamicina, iako se ovi nalazi moraju potvrditi u neovisnim studijama obzirom na preklapanje biogeneze ova dva kompleksa. Temeljem ovih nalaza protokoli doziranja rapamicina modificirani su na način da se mTORC2 ne uvede u inhibiciju produženim djelovanjem rapamicina kako bi se izbjegli njegovi negativni učinci. Većina istraživanja ipak je napravljena na mTORC1, na kojem je i dokazan učinak rapamicina u produljenju životnog vijeka nižih organizama. Ovaj je učinak dokazan direktnom primjenom rapamicina ali i kroz genetičke studije u kojima su mete na koje rapamicin djeluje, odnosno molekule koje se nalaze u signalnom putu mTOR1, mutirane čime je zapravo dobiven isti ishod.
Koja je uloga mTORC-a u stanici? Ovo je pitanje još uvijek otvoreno budući da se radi zapravo o velikom proteinskom kompleksu koji stupa u interakciju sa stotinama drugih različitih proteina u stanici a priroda većine tih interakcija nije ni približno razjašnjena. Najjednostavnije rečeno sve su to proteini koji sudjeluju u izgradnji ili razgradnji staničnih elemenata.
U kontekstu starenja, vjerojatno je bitnija njegova uloga u procesima razgradnje jer se njima iz stanice eliminiraju oštećene i islužene komponente te tako stanica održava svoju vitalnost. Za njegovu funciju bitan je i smještaj u lizosomima budući da se radi o organelima koji djeluju kao svojevrsna reciklažna dvorišta u stanici. U širem kontekstu tkiva, kompleksi mTORa prisutni su u svim tkivima i moglo bi se reći kako se zapravo radi o proteinu koji je bitan za bazične funkcije stanice.
Koliko još moramo naučiti o rapamicinu govore i rezultati istraživanja provedenog na štakorima u kojem se predviđalo negativno djelovanje rapamicina na mišićnu masu kod starijih glodavaca, no rezultati nisu potvrdili to očekivanje. Ideja je bila da inhibicija mTOR kompleksa sprečava anabolizam, odnosno izgradnju mišića, što dugoročno mora rezultirati gubitkom mišićne mase. Ovaj nalaz može se objasniti time da se u djelovanju rapamicina na mTOR ne radi o „pali-gasi“ mehanizmu već da optimalna funkcija mTOR kompleksa ovisi o tome da rapamicina ne bude ni previše ni premalo, zapravo točno u nekom optimalnom rasponu (još ne znamo koji bi to bio), kada možemo dobiti sve koristi njegovog djelovanja bez negativnih nuspojava kao što je gubitak mišićne mase. Njena izgradnja je bitna ako želimo rapamicin koristiti kao geroprotektivni agens jer je poznato da je mišićna masa u starijoj dobi jedan od najvažnijih čimbenika održavanja vitalnosti.
Slična istraživanja provedena su za drugi spoj s potencijalom u georoprotekciji, metformin, gdje se pokazalo da on negativno djeluje na porast mišićne mase prilikom vježbanja, no opet, postavlja se pitanje životnog perioda, vrste vježbanja i doze koja na taj način utječe. Postoje različite spekulacije o tome kako je moguće da rapamicin na kraju ipak ima neto pozitivan učinak unatoč inhibiciji anaboličke funkcije mTOR1. Naime, pretpostavlja se kako osim u ovim procesima, mTOR1 sudjeluje i u procesima kronične upale koji oštećuju tkiva a koji su sve prisutniji što je organizam stariji, te da inhibicija mTOR1 djeluje protuupalno te možda ima na kraju učinak smanjenog oštećenja mišića, ako već ne pomaže njegovoj izgradnji. Iz ovog primjera je vidljivo kako niti pretpostavke izvedene na temelju nekih spoznaja o djelovanju rapamicina na kraju, kada se gleda njegov neto učinak, ne moraju biti potvrđene. Stoga je jasno zašto je teško istraživati molekule sa svojstvom geroprotekcije u tako kompleksnim sustavima.
Od prvotnog zazora od rapamicina kao imunospresora, daljnjim istraživanjima pokazano je da je, primjerice u jednoj studiji, odgovor starijih osoba koje su prethodno bile neko vrijeme na rapamicinu na cjepivo protiv gripe bio značajno bolji u odnosu na one koji nisu uzimali rapamicin. Postavilo se pitanje, kako to jedan notorni imunosupresor, jer uostalom, tome je prvotno i služio, odjednom može imati takva svojstva. Daljnim studijama pokazano je da on utječe na epigenetski profil stanica imunološkog sustava te da ih „podmlađuje“ budući da su osobe koje su uzimale rapamicin imale obrasce metilacije gena (epigenetski biljeg) po statusu bliže osobama puno mlađe životne dobi. No, postavlja se pitanje je li „epigenetski sat“ dobar marker starenja budući da gotovo svaka stvar može utjecati na njega i to prolazno i reverzibilno. Direktna veza između rapamicina i epigenetskih biljega starenja također nije dokazana, već su ovo sve bili posredni dokazi.
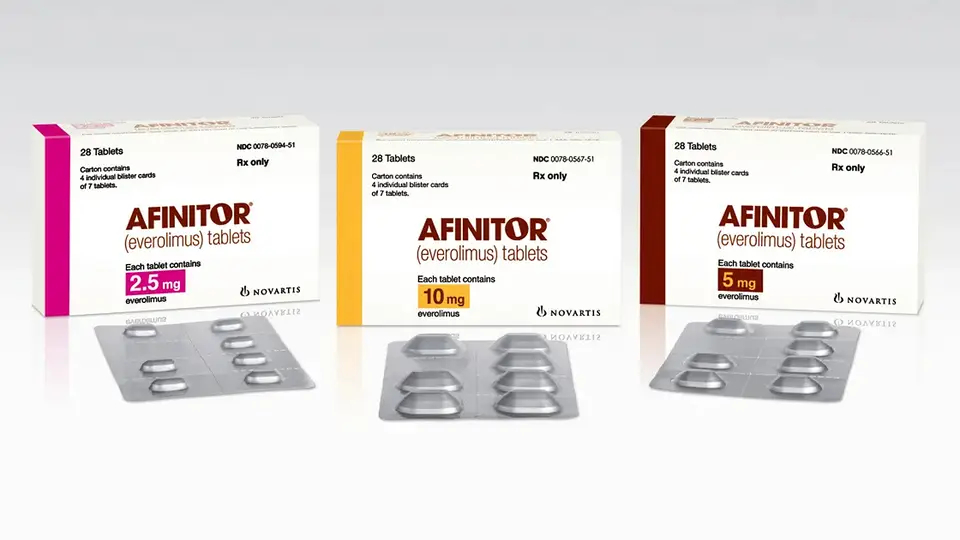
Modifikacija rapamicina komercijalnog naziva Everolimus kao i niz drugih kemijskih derivata rapamicina tzv. „rapaloga“ radi slične stvari kao rapamicin ali mu je biodostupnost bolja te je zato komercijaliziran. Dijelom se te modifikacije rade i kako bi se produžila patentna prava na lijekove koji se na njima temelje iako u suštini imaju isti učinak. Everolimus se koristi kao antitumorski lijek što je još jedno od svojstava rapamicina. U odnosu na rapamicin, everolimus djeluje selektivnije na kompleks mTORC1 dok je njegov učinak na mTORC2 minimalan. Inhibicija mTORC1 po principu negativne povratne sprege izaziva pojačanu aktivaciju kinaze Akt koja se trudi aktivirati mTORC1 ali to ne uspijeva jer je on blokiran. Istovremeno kompleks mTORC2 i dalje reagira na Akt pa se i s te strane izbjegavaju negativni učinci koje izaziva rapamicin. Ako dakle pridodamo protutumorski učinak rapamicina učinku podmlađivanja stanica onda svakako možemo reći kako ova molekula barem u teoriji ima potencijal djelovati kao geroprotektor.
Na kraju treba reći da se životni vijek kontinuirano produžuje već unatrag dvije stotine godina, no s time paralelno raste i incidencija bolesti povezanih sa starenjem poput neurodegenerativnih bolesti. Stoga produljenje životnog vijeka bez produljenja perioda u kojem ćemo biti zdravi i funkcionalni nema previše smisla. Upravo supstance koje bi mogle usporiti procese starenja, djelovati pozitivno na čišćenje stanica od „smeća“ te one koje bi imale protuupalne i protutumorske učinke stoga izazivaju veliki interes. Čak i kada bi se nedvojbeno dokazali učinci geroprotektora, postavlja se pitanje kada bi ih trebalo početi primjenjivati, jer znamo da proces starenja započinje našim rođenjem. Stoga je ideja primjene neke supstance kroz desetljeća jasno primamljiva farmaceutskoj industriji, no kako osmisliti studije koje bi takve učinke nedvojbeno potvrdile, sasvim je drugo pitanje.
1) Mafi S, Mansoori B, Taeb S, Sadeghi H, Abbasi R, Cho WC, Rostamzadeh D. mTOR-Mediated Regulation of Immune Responses in Cancer and Tumor Microenvironment. Front Immunol. 2022; 12:774103. doi: 10.3389/fimmu.2021.774103.
2) López-Otín C, Blasco MA, Partridge L, Serrano M, Kroemer G. Hallmarks of aging: An expanding universe. Cell. 2023;186(2):243-278. doi: 10.1016/j.cell.2022.11.001. Epub 2023 Jan 3.
3) Mannick JB, Del Giudice G, Lattanzi M, Valiante NM, Praestgaard J, Huang B, Lonetto MA, Maecker HT, Kovarik J, Carson S, Glass DJ, Klickstein LB. mTOR inhibition improves immune function in the elderly. Sci Transl Med. 2014;6(268):268ra179. doi: 10.1126/scitranslmed.3009892.
4) Juricic P, Lu YX, Leech T, Drews LF, Paulitz J, Lu J, Nespital T, Azami S, Regan JC, Funk E, Fröhlich J, Grönke S, Partridge L. Long-lasting geroprotection from brief rapamycin treatment in early adulthood by persistently increased intestinal autophagy. Nat Aging. 2022;2(9):824-836. doi: 10.1038/s43587-022-00278-w.