-
Naslovna fotografija: Apstraktni mozaik stanica raka, molekula DNA i ljudskih tkiva. (Midjourney v7)
-
Dr. sc. Tamara Čačev viša je znanstvena suradnica u Zavodu za molekularnu medicinu Instituta Ruđer Bošković. Čačev je također članica Savjeta Ideje.hr
Naslov današnjeg teksta prilično je kontroverzan jer nekako je logično da što više imaš parametara kojim možeš opisati neki sustav, bolje ga možeš razumijeti i predvidjeti njegovo ponašanje. Iz te je pretpostavke nastala i ideja “precizne medicine“ koja je posebno dobila zamaha u području onkologije. Naime, razvoj modernih tehnologija molekularne biologije, poput sekvenciranja genoma, potaknuo je (optimistično) uvjerenje da će detaljna molekularna karakterizacija tumora omogućiti preciznu i predvidivu terapijsku intervenciju. Razvoj metoda tekuće biopsije otvorio je mogućnost detekcije tumorske DNA u krvi potencijalno i prije detekcije samog tumora. Umjetna inteligencija danas analizira histološke preparate i radiološke slike na razini koja konkurira, a moguće uskoro i nadilazi, ekspertizu pojedinca. Stoga nije čudno to što se na molekularnu podlogu nastanka tumorskih bolesti počelo gledati, kao i na mnogo toga prije u znanosti, kao na problem koji je moguće riješiti dovoljno preciznim mjerenjem i opisivanjem nizom parametara. Ideja “precizne onkologije“ jest da identifikacijom ključnih mutacija i signalnih puteva možemo precizno intervenirati i zaustaviti tumor i njegove metastaze.
No, možemo li s dovoljno “izmjerenih“ parametara u danom trenutku, uistinu spoznati neko buduće ponašanje kompleksnog sustava kao što je tumor? Mogu li se kompleksni sustavi ikad dovoljno dobro modelirati kako bi predvidjeli njihovu budućost duže od kratkog vremena nakon samog mjerenja?
Iako smo kompleksnost tumora poznavali i ranije, napredak navedenih tehnologija pruža nadu da možemo mjeriti i pratiti njegovu dinamičku prirodu; kako se mijenja kroz vrijeme i prilagođava terapiji te kako koristi vlastitu heterogenost kao mehanizam preživljavanja. Zahvaljujući napretku možemo reći da onkologija danas gotovo da više i nema problem nedostatka podataka, već se mora uhvatiti u koštac s njihovom interpretacijom. Jer, kako to obično biva s kompleksnim sustavima, što preciznije mjerimo tumor, to je jasnije da ga nije moguće objasniti jednim modelom ni kontrolirati jednom terapijskom metom. Nažalost, unatoč opisanom napretku na strani mjerenja, klinički ishodi nisu proporcionalno poboljšani. Odgovori na ciljane terapije često su kratkotrajni, rezistencija na terapiju se i dalje razvija, a mnoge molekularne informacije i dalje nisu popraćene adekvatnim terapijskim odgovorom. Analiza koju su 2018. godine proveli Marquart i surardnici pokazala je da je udio oboljelih s uznapredovalom tumorskom bolesti koji ostvaruju klinički benefit od genomikom vođene terapije relativno nizak (oko 8–10%) u SAD-u (Marquart et al., 2018). Iako se taj postotak povećava s razvojem novih lijekova, i dalje ukazuje na značajan jaz između molekularne detekcije i terapijske učinkovitosti.
Čak i u slučajevima gdje su identificirani jasni “driver” onkogeni koji pokreću nastanak i napredovanje nekog tumora, te su razvijeni učinkoviti inhibitori, trajanje odgovora često je ograničeno. Mehanizmi rezistencije su višeslojni i uključuju genetske i negenetske komponente. Na genetskoj razini, sekundarne mutacije u genu čiji produkt je meta ciljane terapije ili aktivacija alternativnih signalnih puteva omogućuju zaobilaženje inhibiranog puta. Dodatno, negenetski mehanizmi poput epigenetskog reprogramiranja i fenotipske plastičnosti tumora igraju ključnu ulogu u ranoj fazi adaptacije na terapiju. Poseban problem predstavlja mrežna redundancija signalnih puteva. Tumor nije sustav koji se može trajno destabilizirati inhibicijom jedne molekularne mete već se radi o čitavoj mreži signalnih puteva koja reorganizira svoju funkciju kao odgovor na terapijski pritisak. Zato i govorimo o svojevrsnoj evoluciji tumora. Inhibicija jednog čvora u signalnoj mreži često dovodi do kompenzatorne aktivacije paralelnih ili povratnih puteva. Također, velik broj identificiranih mutacija u tumorima koje su sve potencijalno na prvu moguće mete za razvoj novih terapija u kliničkom kontekstu ne dovode do značajnog produljenja preživljenja. Razlozi uključuju nisku ovisnost tumora o toj mutaciji, heterogenost tumora te farmakodinamička i farmakokinetička ograničenja lijekova. Tumori funkcioniraju kao robusni sustavi s ugrađenim mehanizmima otpornosti na promjene.
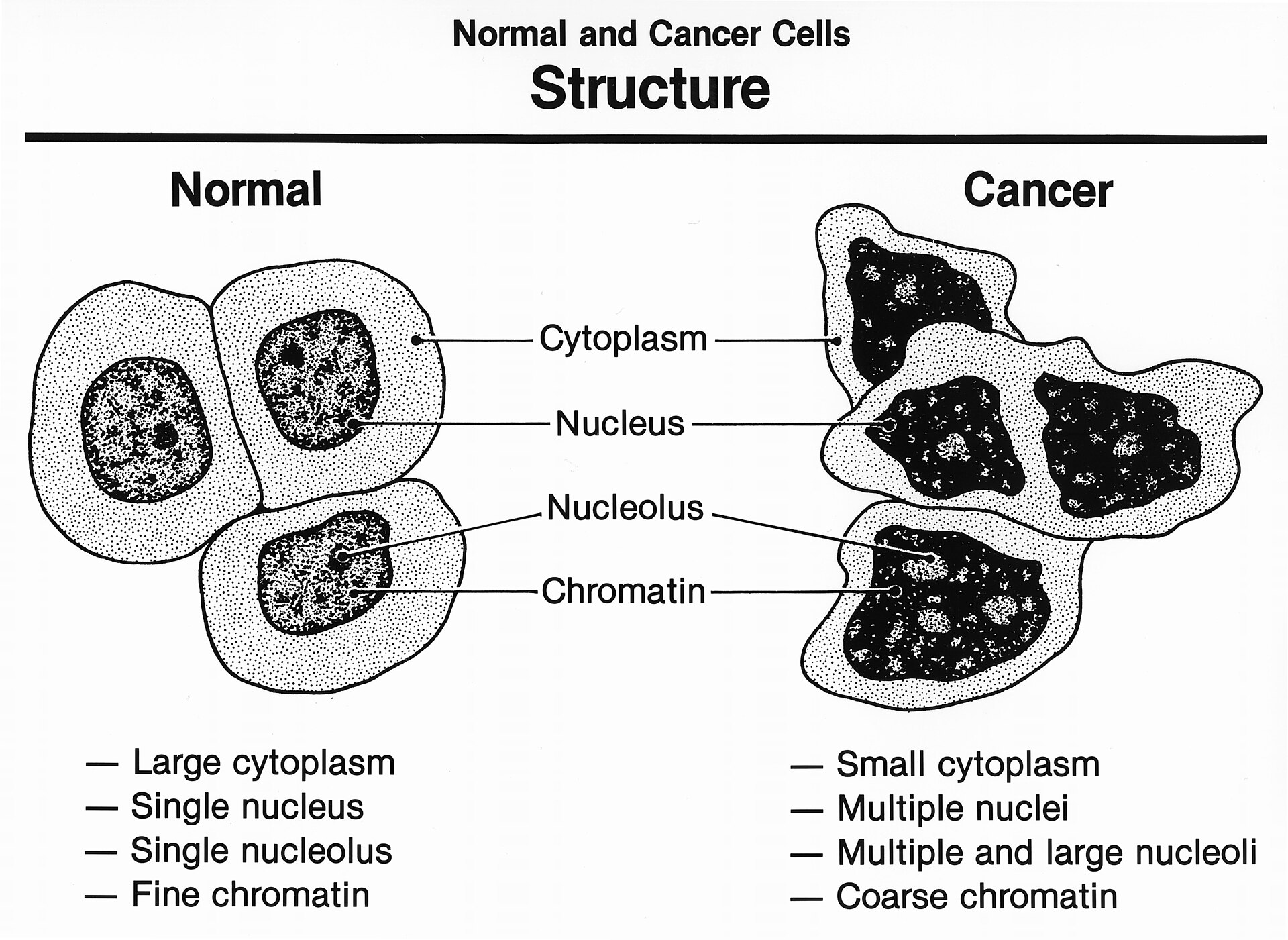
Normalne stanice s lijeve strane i stanice raka s desne, s karakterističnim strukturama. (Pat Kenny, CC0)
Iz svega proizlazi da je glavno ograničenje precizne onkologije u implicitnoj pretpostavci linearne kauzalnosti. Klasični model nastanka i napredovanja tumora kojeg su predložili Fearon i Vogelstein, temelji se na pretpostavci da su somatske mutacije primarni pokretači tumorigeneze. U vrijeme nastanka tog modela identifikacija niza onkogena i tumorsupresorskih gena omogućila je razumijevanje ključnih signalnih puteva uključenih u proliferaciju i preživljenje stanica. Ovaj model bio je iznimno produktivan za razvoj molekularne onkologije te je i doveo do razvoja prvih ciljanih terapija.
Međutim, suvremena istraživanja pokazuju da genetske promjene same po sebi ne mogu objasniti kompleksnost tumorskog fenotipa. Funkcionalni učinak mutacije ovisi i o kontekstu u kojem ona djeluje, uključujući epigenetsko stanje stanice, dostupnost metaboličkih resursa i interakcije s mikrookolišem. Na najosnovnijoj razini, mutacija predstavlja promjenu u DNA sekvenci. Međutim, između nečega što je kodirano u DNA i tumorskog fenotipa nalazi se složeni sustav regulacije ekspresije gena. Epigenetski mehanizmi, uključujući DNA metilaciju, modifikacije histona i organizaciju kromatina, određuju koji će geni biti aktivni, u kojem intenzitetu i u kojem vremenskom “prozoru“. To znači da ista mutacija može imati različit funkcionalni učinak ovisno o tome nalazi li se u stanici s “otvorenim” ili “zatvorenim” kromatinskim stanjem. Primjerice, onkogeni signal može ostati funkcionalno utišan ako je smješten u epigenetskom kontekstu koji ograničava ekspresiju njegovih efektorskih gena (gena na koje bi on dalje trebao djelovati). Suprotno tome, u epigenetski permisivnom okruženju ista mutacija može imati snažan proliferativni učinak. Ova razina regulacije također omogućuje reverzibilnost budući da su, za razliku od genetskih mutacija, epigenetske promjene potencijalno promjenjive, što ima također i važne terapijske implikacije. Nadalje, tumorske stanice aktivno reprogramiraju svoje metaboličke puteve kako bi zadovoljile potrebe za energijom i biosintezom. Mutacije u onkogenima poput MYC ili KRAS često imaju svoj primarni učinak upravo kroz promjene u metabolizmu kao što je primjerice povećanje unosa glukoze, ovisnost o glutaminu ili aktivaciju tzv. jednougljičnih (one-carbon) puteva. Međutim, dostupnost tih metaboličkih resursa nije konstantna, nego ovisi o lokalnom mikrookolišu, vaskularizaciji i kompeticiji s drugim stanicama. Stoga učinak mutacije može varirati ovisno o metaboličkom “ekosustavu” u kojem se stanica nalazi. Tumor nije izolirana masa isključivo tumorskih stanica već sadrži i druge tipove stanica kao što su fibroblasti, imunološke stanice, krvne žile i ekstracelularni matriks koje tvore tzv. mikrookoliš tumora. Ove komponente aktivno sudjeluju u regulaciji tumorskog ponašanja. Na primjer, stromalne stanice mogu lučiti čimbenike rasta koji kompenziraju inhibiciju signalnih puteva unutar tumorske stanice, dok imunološke stanice mogu ili suprimirati ili poticati tumorski rast, ovisno o svom funkcionalnom stanju. U tom kontekstu, mutacija nije jedina promjena koja je bitna za tumorigenezu, već proliferacija, invazija, metastaziranje ili terapijska rezistencija tumora, osim o samim tumorskim stanicama, ovise i o kontekstu mikrookoliša u kojem se nalaze.
Tako dolazimo do ključnog problema – ako je učinak mutacije kontekstualno uvjetovan, tada terapija koja cilja na tu mutaciju ne može biti univerzalno učinkovita. Uspjeh terapije ovisit će o tome u kojoj mjeri je tumor “ovisan” o tom signalnom putu u konkretnom biološkom okruženju. To objašnjava zašto ista molekularna meta može imati dramatično različite kliničke učinke u različitim tumorima, ali i među oboljelima s nominalno istim molekularnim profilom. Primjerice, mutacija BRAF V600E ima dramatično različite terapijske implikacije ovisno o tipu tumora. U melanomu inhibicija BRAF-a dovodi do značajnih kliničkih odgovora, dok u tumorima debelog crijeva isti pristup pokazuje ograničenu učinkovitost zbog kompenzatorne aktivacije EGFR signalnog puta.
Kada se fokusiramo isključivo na tumorske stanice unutar tumora, dolazimo do toga da se ne radi o istovjetnim stanicama već o različitim klonovima sa specifičnim genetskim, epigenetskim i fenotipskim karakteristikama. Ova intratumorska heterogenost ima duboke kliničke implikacije. Naime, standardna biopsija tumora uzorkuje obično samo jedan mali dio tumora i time pruža parcijalnu sliku njegove molekularne arhitekture. Rezultat je dijagnostička redukcija kompleksnog sustava na jedan “snapshot” koji ne odražava punu raznolikost tumora. Rezistentni klonovi, koji mogu biti prisutni u malom broju u trenutku dijagnoze, često ostaju nedetektirani, ali postaju dominantni pod terapijskim pritiskom. Dodatno, stanice unutar tumora nisu raspoređene nasumično već su organizirane u funkcionalne “niše“ koje uključuju interakcije s fibroblastima, imunološkim stanicama i ekstracelularnim matriksom. Ove prostorne interakcije mogu modulirati osjetljivost na terapiju i doprinijeti heterogenosti odgovora.
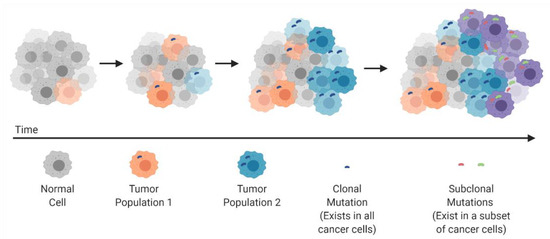
Klonalna evolucija tumora i razvoj heterogenosti. (MDPI, CC0)
Razvoj tehnika poput single-cell sekvenciranja i prostorne transkriptomike omogućio nam je da probamo doskočiti multidimenzionalnosti tumorskih bolesti. Single-cell RNA sekvenciranje (scRNA-seq) omogućuje mjerenje ekspresije gena u pojedinačnim stanicama, umjesto u mješavini tisuća ili milijuna stanica. Tehnički, proces uključuje izolaciju pojedinačnih stanica iz tumorskog tkiva, njihovo razbijanje kako bi se došlo do molekula RNA koje se zatim prevode u cDNA i sekvenciraju, pri čemu svaka stanica dobiva svoju svojevrsnu barkod oznaku kako bi se na temelju toga dobila preciznija distribucija staničnih stanja unutar tumora. Na ovaj način mogu se detektirati različite tumorske subpopulacije (npr. proliferativne, invazivne, metabolički adaptirane), zatim stanice u različitim fazama diferencijacije kao i kompleksne populacije stromalnih i imunoloških stanica. Primjerice, unutar nekog solidnog tumora mogu koegzistirati stanice s izraženim “stem-like” karakteristikama, visoko diferencirane epitelne stanice te stanice u EMT stanju. Ove populacije imaju različitu osjetljivost na terapiju, što objašnjava zašto tumori često ne reagiraju uniformno.
I dok je single-cell sekvenciranje odgovorilo koje sve stanice postoje u tumoru, prostorna transkriptomika odgovara na pitanje gdje se te stanice nalaze i kako su organizirane. Naime, klasični single-cell pristup zahtijeva razgradnju tumorske mase do razine pojedinačnih stanica čime se gubi informacija o njihovom prostornom rasporedu. Prostorna transkriptomika preskaće ovu prepreku jer omogućuje mjerenje ekspresije gena in situ čime tkivni kontekst ostaje očuvan. RNA iz svake mikrolokacije veže se za specifične oznake, čime se omogućuje rekonstrukcija prostorne distribucije ekspresije gena. Na ovaj način dolazimo do svojevrsne molekularne karte tumora na kojoj identificiramo pojedine regije bogate proliferativnim stanicama, hipoksične zone s metaboličkom adaptacijom, imunološki “hladne” i “vruće” zone te invazivne fronte tumora. Primjerice, na invazivnom rubu tumora često se nalaze stanice u EMT stanju koje interagiraju s fibroblastima i remodeliraju ekstracelularni matriks. U centralnim dijelovima tumora dominiraju stanice prilagođene hipoksiji i ograničenim resursima. Stanice koje se nalaze u blizini krvnih žila imaju bolju dostupnost kisika i lijekova, dok hipoksične regije često pokazuju rezistenciju. Slično, prisutnost imunoloških stanica može povećati učinkovitost imunoterapije, ali samo ako su funkcionalno aktivne. Fibroblasti (CAF-ovi), imunološke stanice i tumorski epitel ne djeluju u izolaciji već komuniciraju putem citokina, kemokina i kontaktnih signala. Ove interakcije mogu poticati rast tumora, inducirati rezistenciju ili modulirati imunološki odgovor. Razlike koje nastaju unutar tumora nisu nasumične, nego nastaju kao rezultat lokalnih selekcijskih pritisaka. To znači da terapija koja cilja jedan dio tumora može biti neučinkovita u drugom dijelu. Ipak, ove tehnologije i dalje ne rješavaju problem kompleksnosti tumora niti kako to terapijski iskoristiti. I dalje je riječ je o snapshot pristupu, koji ne hvata dinamičke promjene kroz vrijeme, niti evoluciju tumora pod terapijskim pritiskom. Konačno, njihova klinička primjena zasad je ograničena zbog cijene, standardizacije i nedostatka validiranih terapijskih implikacija, što znači da još uvijek rijetko mijenjaju konkretne odluke u liječenju oboljelih.
Tumor se također može promatrati kao evolucijski sustav koji podliježe principima darvinističke selekcije. Genetska varijabilnost unutar tumora stvara populaciju stanica s različitim adaptivnim potencijalima. Terapija djeluje kao selekcijski pritisak koji eliminira osjetljive stanice, dok rezistentne populacije preživljavaju i proliferiraju. Pri tome rezistencija nije nužno rezultat novih mutacija nastalih tijekom terapije. Često je riječ o selekciji već postojećih subklonova ili o fenotipskoj plastičnosti koja omogućuje stanicama da promijene svoje stanje bez genetskih promjena. Procesi poput epitelno-mezenhimalne tranzicije (EMT) omogućuju stanicama da steknu invazivna i rezistentna svojstva, dok promjene u metaboličkom programu omogućuju prilagodbu na terapijske i okolišne uvjete. Tijekom epitelno-mezenhimalne tranzicije, epitelne stanice gube međustanične spojeve i polaritet, a stječu migratorna i invazivna svojstva što im omogućuje diseminaciju i često povećava otpornost na terapiju.
Paralelno s time, tumorske stanice aktivno reprogramiraju svoj metabolizam i prelaze između različitih izvora energije i biosintetskih puteva, ovisno o dostupnosti resursa i terapijskom pritisku. Tako mogu, primjerice, smanjiti ovisnost o glukozi i povećati korištenje glutamina ili drugih supstrata, čime održavaju rast i preživljenje u nepovoljnim uvjetima. Ovi procesi zajedno omogućuju fenotipsku plastičnost – sposobnost stanice da mijenja svoje stanje bez promjene genetskog koda što objašnjava zašto se rezistencija često razvija i u odsutnosti novih mutacija.
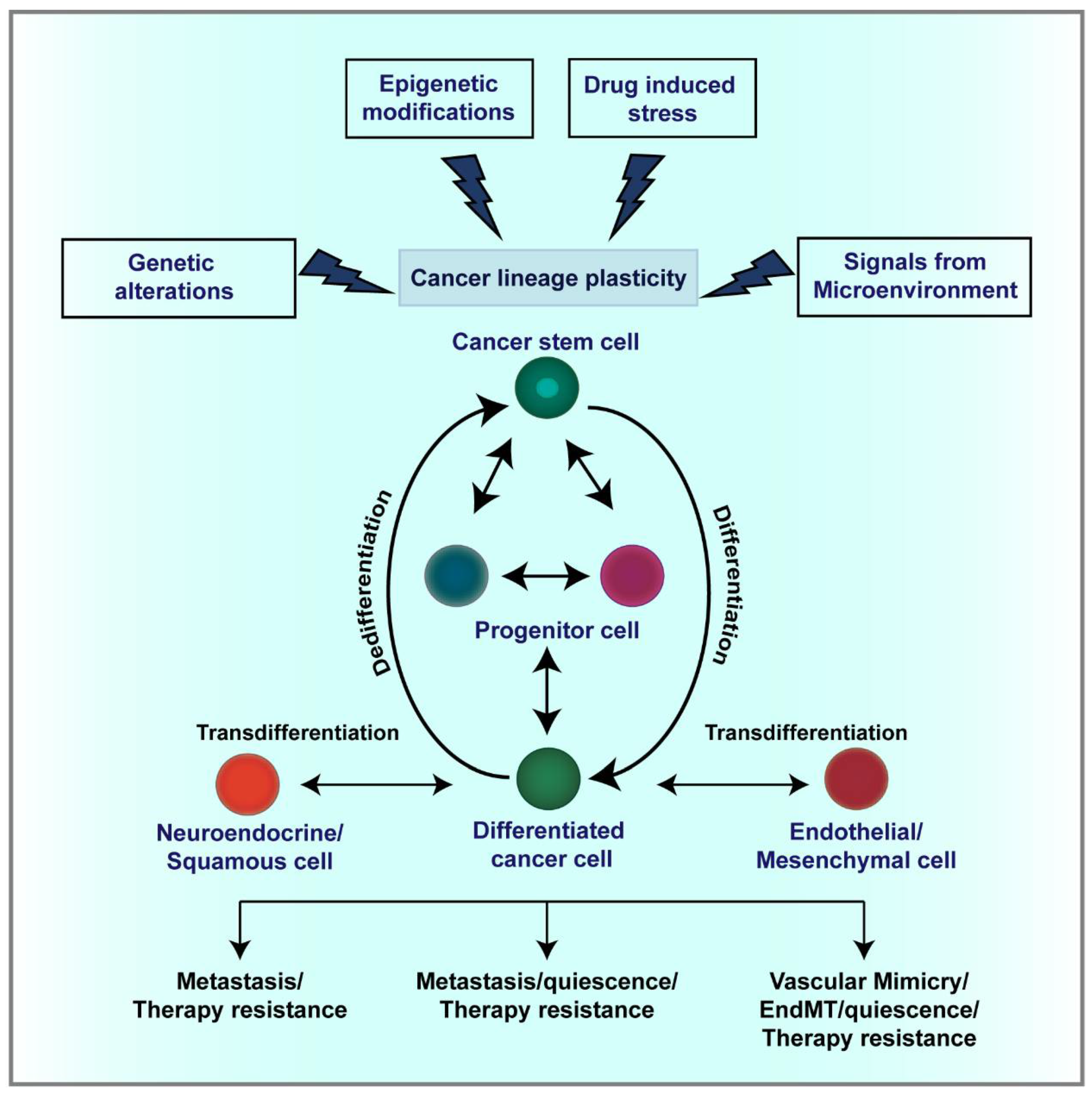
Plastičnost tumorskih stanica potiče napredovanje tumora, otpornost na terapiju i metastaze. (MDPI, CC0)
Danas znamo i da unatoč velikom broju identificiranih mutacija, samo manji dio njih ima izravnu terapijsku implikaciju. Još manje tih mutacija rezultira dugotrajnim kliničkim odgovorom. Razlog tome je u tome što je većina tumora pogonjena kompleksnim mrežama signalnih puteva, a ne jednim dominantnim driverom. Inhibicija jednog puta često dovodi do aktivacije alternativnih mehanizama, čime se održava tumorska funkcija. Ovaj fenomen mrežne redundancije predstavlja temeljno ograničenje ciljanih terapija. Dodatno, sve je jasnije da tumorske stanice često nisu “ovisne” o jednoj mutaciji onoliko koliko se pretpostavljalo, a radi se o fenomenu koji se u anglosaksonskoj literaturi naziva non-oncogene addiction i implicira da je njihov opstanak rezultat koordinirane aktivnosti više signalnih i metaboličkih programa, a ne jednog dominantnog mehanizma. Posljedično, i kada identificiramo molekularnu metu i razvijemo lijek koji je učinkovito inhibira, tumor može zadržati funkcionalnost kroz reorganizaciju svoje signalne mreže. Stoga, postojanje mutacije za koju možemo razviti neku molekularnu terapiju ne znači nužno i kliničku korist, jer terapijski učinak ovisi o tome koliko je konkretni tumor zaista funkcionalno ovisan o tom putu, što je svojstvo sustava, a ne pojedinačne molekule.
Razvoj metoda tekuće biopsije omogućio je identifikaciju tumorskih promjena u vrlo ranim fazama. Ove metode mogu identificirati vrlo male količine mutiranih fragmenata DNA u krvi, često i prije nego što se tumor može detektirati radiološki ili klinički. No, detekcija molekularnih promjena ne znači nužno prisutnost klinički relevantne bolesti. Dodatno, mutacije detektirane u krvi mogu potjecati iz benignih klonalnih ekspanzija, poput klonalne hematopoeze povezane sa starenjem. Također, čak i kada mutacije potječu iz stvarnih tumorskih lezija, ostaje pitanje njihove biološke sudbine. Nisu svi tumori progresivni, neki ostaju stabilni ili se razvijaju izuzetno sporo. Sve to ukazuje na temeljni problem, a to je da granica između “zdravog” i “bolesnog” na molekularnoj razini nije oštra, nego kontinuirana. Kako tehnologije postaju osjetljivije, sve češće detektiramo promjene koje pripadaju tom intermedijarnom prostoru između normalne biološke varijacije i manifestne bolesti. Iz toga proizlazi da interpretacija i stratifikacija rizika postaju iznimno bitne u ovoj novoj eri koja nas zasipa nizom molekularnih informacija.
S obzirom na sve navedeno sve se veći naglasak stavlja na dinamički pristup praćenja tumora koji se temelji na njegovom kontinuiranom praćenju kroz vrijeme što omogućuje detekciju promjena u realnom vremenu i prilagodbu terapije. Također se rađa i novi koncept adaptivne terapije koji se temelji na ideji da je održavanje populacije osjetljivih stanica (umjesto totalnog uništenja tumora) korisno jer one konkuriraju rezistentnim klonovima i sprječavaju njihovu dominaciju. Ovaj pristup koristi principe evolucijske biologije kako bi se bolest držala pod kontrolom.
Ipak, iako ciljani lijekovi nisu jednako učinkoviti u svim vrstama tumora u nekim tumorskim podskupinama s jasno definiranim molekularnim “driverom”, te kada se lijek primjenjuje na temelju specifičnih biomarkera, usko selektiranoj populaciji mogu bitno promijeniti tijek bolesti. Najdramatičniji primjer je kronična mijeloična leukemija, u kojoj su BCR::ABL1 inhibitori bolest iz nekoć smrtonosne pretvorili u kroničnu. Tehnologija omogućuje neviđenu razinu detalja u opisu tumora te će daljnji napredak ovisiti o sposobnosti integracije podataka u modele koji odražavaju dinamičku i višerazinsku prirodu bolesti. Čini se da onkologija ulazi u fazu u kojoj tehnologija više nije ograničavajući čimbenik, već ograničenje postaje naše razumijevanje kompleksne biologije tumorskih sustava.
Marquart J, Chen EY, Prasad V. Estimation of the Percentage of US Patients With Cancer Who Benefit From Genome-Driven Oncology. JAMA Oncol. 2018 Aug 1;4(8):1093-1098. doi: 10.1001/jamaoncol.2018.1660.
Soragni A, Knudsen ES, O’Connor TN, Tognon CE, Tyner JW, Gini B, Kim D, Bivona TG, Zang X, Witkiewicz AK, Goodrich DW, Jiang D, Gammon ST, Willey CD, Boutros PC, Sandulache VC, Osman AA, Myers JN, Mehla K, Singh PK, Chan KS, Gao H, Marathe H; National Cancer Institute (NCI) Acquired Resistance to Therapy Network (ARTNet). Acquired resistance in cancer: towards targeted therapeutic strategies. Nat Rev Cancer. 2025 Aug;25(8):613-633. doi: 10.1038/s41568-025-00824-9.
Fearon ER, Vogelstein B. A genetic model for colorectal tumorigenesis. Cell. 1990 Jun 1;61(5):759-67. doi: 10.1016/0092-8674(90)90186-i.
Hanahan D, Weinberg RA. The hallmarks of cancer. Cell. 2000 Jan 7;100(1):57-70. doi: 10.1016/s0092-8674(00)81683-9.
Hanahan D. Hallmarks of Cancer: New Dimensions. Cancer Discov. 2022 Jan;12(1):31-46. doi: 10.1158/2159-8290.CD-21-1059.
Hanahan D. Hallmarks of cancer-Then and now, and beyond. Cell. 2026 Jan 29:S0092-8674(25)01498-9. doi: 10.1016/j.cell.2025.12.049.